Giới thiệu tổng quan
Phản ứng giữa sắt (Fe) và đồng (II) nitrat (Cu(NO3)2) là một trong những phản ứng hóa học cơ bản nhưng có nhiều ứng dụng quan trọng trong công nghiệp và đời sống. Bài viết này sẽ đi sâu phân tích các khía cạnh của phản ứng, từ cơ chế diễn ra đến các ứng dụng thực tiễn.
Cơ sở lý thuyết
Phương trình phản ứng
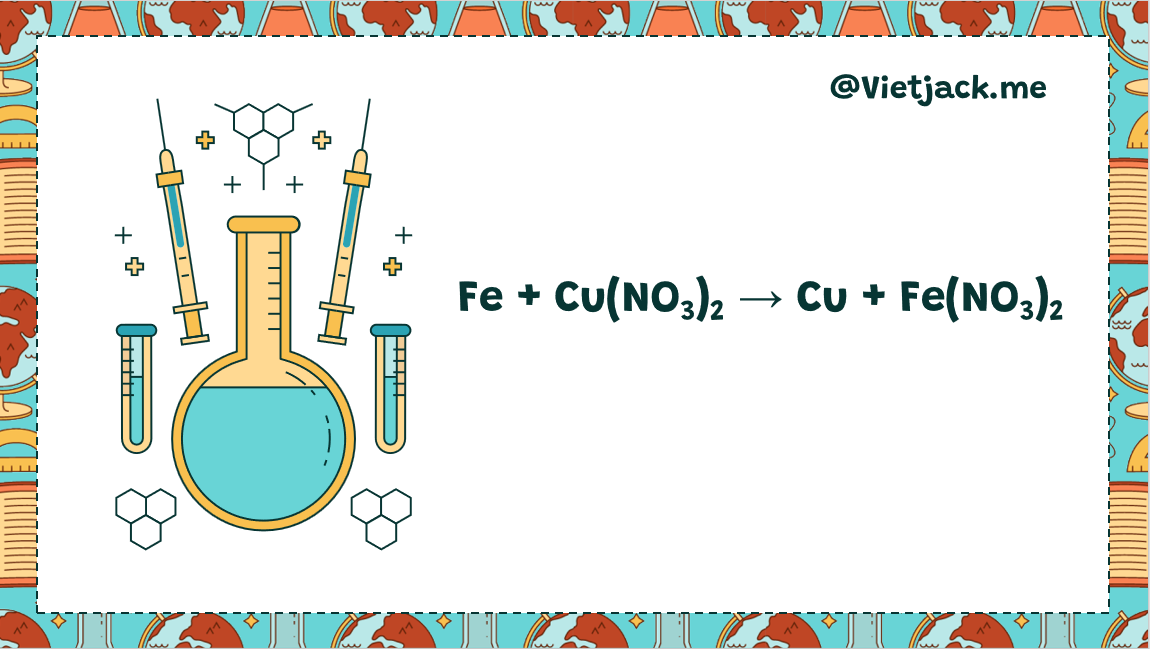
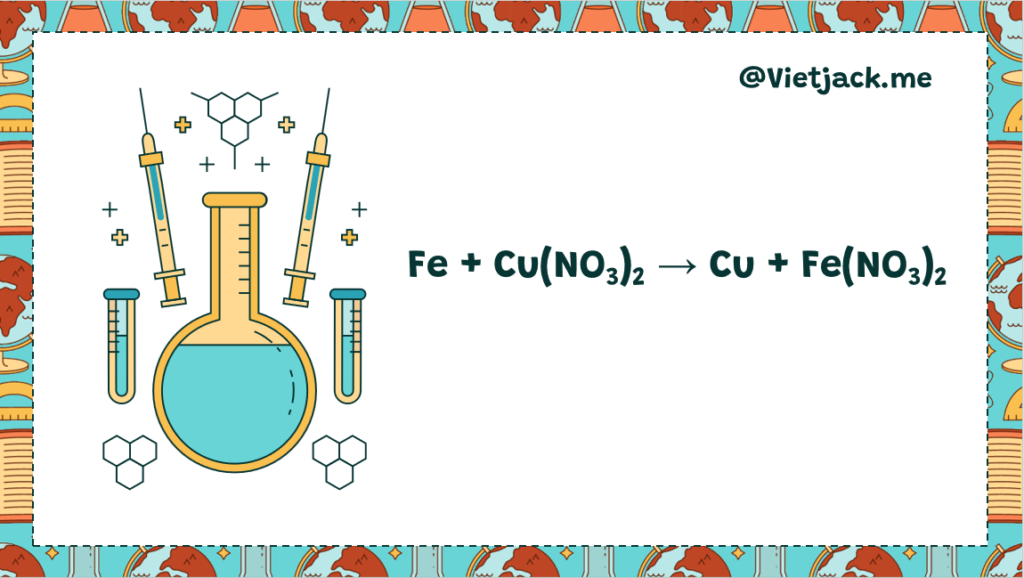
Phản ứng giữa Fe và Cu(NO3)2 diễn ra theo phương trình:
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
Đây là một phản ứng oxi hóa – khử điển hình, trong đó:
- Fe bị oxi hóa thành Fe2+
- Cu2+ bị khử thành Cu
Điều kiện phản ứng
Phản ứng này diễn ra trong điều kiện:
- Nhiệt độ phòng
- Áp suất thường
- Môi trường dung dịch
Cơ chế phản ứng
Quá trình oxi hóa khử
- Bước 1: Fe cho electron
- Fe → Fe2+ + 2e-
- Sắt kim loại bị oxi hóa, nhường 2 electron
- Bước 2: Cu2+ nhận electron
- Cu2+ + 2e- → Cu
- Ion đồng nhận 2 electron và bị khử thành đồng kim loại
Các yếu tố ảnh hưởng
- Nồng độ chất phản ứng:
- Nồng độ Cu(NO3)2 cao sẽ đẩy nhanh tốc độ phản ứng
- Diện tích bề mặt Fe càng lớn, phản ứng càng nhanh
- Nhiệt độ:
- Nhiệt độ tăng làm tăng tốc độ phản ứng
- Mỗi 10°C tăng thêm có thể làm tăng tốc độ phản ứng 2-3 lần
Ứng dụng thực tiễn
Trong công nghiệp
- Sản xuất đồng tinh khiết:
- Tách đồng từ dung dịch muối
- Tinh luyện đồng thô
- Xử lý nước thải:
- Loại bỏ ion đồng từ nước thải công nghiệp
- Giảm ô nhiễm môi trường
- Mạ kim loại:
- Tạo lớp phủ đồng bảo vệ
- Trang trí bề mặt sản phẩm
Trong phòng thí nghiệm
- Thí nghiệm giáo dục:
- Minh họa phản ứng oxi hóa khử
- Học tập về điện hóa
- Nghiên cứu khoa học:
- Nghiên cứu động học phản ứng
- Phát triển vật liệu mới

Các vấn đề an toàn
Phòng ngừa rủi ro
- Bảo hộ cá nhân:
- Đeo găng tay và kính bảo hộ
- Mặc áo phòng thí nghiệm
- Xử lý hóa chất:
- Không để hóa chất tiếp xúc với da
- Tránh hít phải hơi NO2 có thể sinh ra
Xử lý sự cố
- Khi tiếp xúc với da:
- Rửa ngay bằng nhiều nước sạch
- Tham khảo ý kiến bác sĩ nếu cần
- Khi tràn đổ:
- Dùng cát hoặc vật liệu thấm hút
- Thu gom và xử lý đúng quy định
Các nghiên cứu mới
Xu hướng phát triển
- Tối ưu hóa quy trình:
- Cải thiện hiệu suất phản ứng
- Giảm chi phí sản xuất
- Ứng dụng mới:
- Phát triển pin và acquy
- Xử lý môi trường
Thách thức và giải pháp
- Vấn đề môi trường:
- Giảm thiểu chất thải
- Tái chế và tái sử dụng
- Hiệu quả kinh tế:
- Tối ưu hóa chi phí
- Nâng cao chất lượng sản phẩm
Kết luận
Phản ứng Fe và Cu(NO3)2 là một ví dụ điển hình về phản ứng oxi hóa khử với nhiều ứng dụng quan trọng. Việc hiểu rõ cơ chế và các yếu tố ảnh hưởng giúp tối ưu hóa quá trình sử dụng trong thực tiễn. Các nghiên cứu tiếp tục được phát triển nhằm mở rộng phạm vi ứng dụng và nâng cao hiệu quả của phản ứng này.
Thông tin thêm:
Vietnam Hackademics cập nhật thông tin mới nhất về hóa học và các lĩnh vực khoa học khác tại vietnamhackademics.org
Thông tin liên hệ:
- Hotline: 0919 29 39 49
- Email: [email protected]
- Website: vietnamhackademics.org
Bài viết được cung cấp bởi Vietnam Hackademics – Nền tảng chia sẻ kiến thức khoa học hàng đầu Việt Nam.